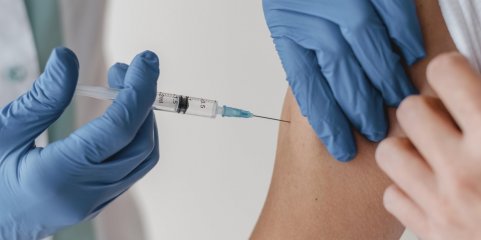
Nova lei de ensaios clínicos garante medicamentos gratuitos e reforça proteção dos participantes
A legislação que regula os ensaios clínicos de medicamentos para uso humano e altera a lei da investigação clínica, hoje publicada em Diário da República, garante medicamentos gratuitos após a investigação e reforça proteção dos participantes.
A nova lei, que entra em vigor dentro de 30 dias, assegura a execução em Portugal do regulamento da União Europeia que harmoniza as regras dos ensaios clínicos de medicamentos para uso humano.
Os ensaios clínicos estão sujeitos a autorização prévia por parte da Autoridade Nacional do Medicamento (Infarmed), após a avaliação técnico-científica e ética do pedido de ensaio clínico.
Segundo a legislação, o Infarmed será responsável pelos aspetos técnicos, enquanto a Comissão de Ética para a Investigação Clínica (CEIC) avalia os aspetos éticos, garantindo que todos os procedimentos cumprem prazos e normas europeias.
A autoridade do medicamento pode, por sua iniciativa ou a pedido da CEIC, “suspender ou revogar a autorização para a realização de um ensaio clínico ou exigir ao promotor a alteração de qualquer aspeto do ensaio clínico, quando as condições em que se fundamentou a autorização para realização do ensaio clínico deixarem de estar preenchidas”.
A lei estabelece os medicamentos e dispositivos utilizados nos ensaios devem ser disponibilizados gratuitamente aos participantes durante e após a conclusão do estudo, enquanto o investigador considere indispensável a continuação da sua utilização e não existam alternativas terapêuticas de eficácia e segurança equiparáveis.
A obrigação de o promotor disponibilizar gratuitamente ao participante os medicamentos, e os dispositivos médicos utilizados para a respetiva administração, “mantém-se até à sua efetiva introdução no setor da distribuição e à garantia do seu acesso nos estabelecimentos do Serviço Nacional de Saúde”, nos termos a definir através de portaria da ministra da Saúde, no prazo de 30 dias após a entrada em vigor da lei.
A legislação reforça a proteção dos participantes impondo o consentimento esclarecido, incluindo menores e maiores incapazes de prestar esse consentimento. Nestes casos, a participação só é possível mediante o consentimento de um representante legalmente autorizado.
A participação de menores “só pode ocorrer se, para além do consentimento esclarecido do seu representante legalmente autorizado, for obtido o seu assentimento”, sublinha.
Os menores e adultos incapazes de prestar consentimento esclarecido, que se encontrem em acolhimento institucional, não podem participar num ensaio clínico, salvo se o facto de não participar resultar num “potencial prejuízo ou desvantagem” para os mesmos.
Em situações de emergência, quando o participante “se encontra em risco grave ou imediato para a vida ou integridade física” e não for possível obter o consentimento em tempo útil, pode ser incluído no ensaio de forma excecional, desde que a investigação esteja diretamente relacionada com essa situação clínica, o protocolo tenha aprovação da comissão ética.
A lei determina que deve ser assegurado que “os riscos ou encargos adicionais são mínimos e que exista uma expectativa fundada de benefício direto para o participante, devendo o consentimento esclarecido ser obtido logo que possível”.
Cabe ao promotor e ao investigador responderem, “de forma solidária e independentemente de culpa, pelos danos patrimoniais e não patrimoniais que o ensaio clínico cause ao sujeito do ensaio”, refere.
“O promotor deve obrigatoriamente contratar um seguro destinado a cobrir a responsabilidade civil (…) adequada à natureza e à extensão do risco”, acrescenta.
O Infarmed é a entidade responsável pela fiscalização e controlo dos ensaios, refere a lei, salientando que os estudos realizados sem autorização ou em desconformidade com a lei incorrem em coimas entre os 500 euros e os 750.000 euros.
Podem ainda aplicar-se sanções acessórias, como a suspensão ou interdição de ensaios por até dois anos.

Freguesia açoriana da Luz cria apoio à natalidade com cabaz de 100 euros

Netanyahu confirma tratamento com radioterapia para cancro da próstata que ocultou

PR escolhe Adalberto Campos Fernandes para coordenador do Pacto Estratégico para a Saúde

Toxicologista avisa sobre introdução de novos contaminantes tóxicos no ecossistema

Prazo do concurso para USF C no Lumiar adiado para 14 de junho após pedido de suspensão
Parlamento recomenda ao Governo implementação da terapia fágica
Técnico de sangue detido pela PJ foi proibido de entrar em Coimbra pelo tribunal
Faturação das clínicas dentárias cresce 6,3% em 2025 para 1.875 ME

Liga contra o cancro saúda reposição de benefícios fiscais para doentes oncológicos
Polícia desmantela três farmácias clandestinas no distrito moçambicano de Mocuba
Mais de 84 mil animais vacinados contra a raiva em Timor-Leste